Pengertian
Golongan pada tabel periodik adalah kelompok unsur yang terletak pada satu lajur vertikal yang sama, sedangkan periode adalah kelompok unsur yang terletak pada satu lajur horizontal yang sama.
Rumus
Pola Konfigurasi Elektron Golongan A (Unsur Utama)
Pola Konfigurasi Elektron Golongan B (Unsur Transisi)
Pola Konfigurasi Elektron Golongan Lantanida (Unsur Transisi Dalam)
Pola Konfigurasi Elektron Golongan Aktinida (Unsur Transisi Dalam)
Keterangan:
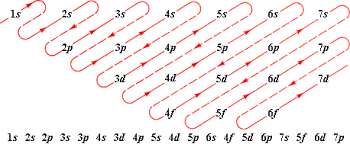
Nomor atom dijabarkan menjadi pangkat konfigurasi elektron berdasarkan urutan di gambar, dengan pangkat s maksimum 2, pangkat p maksimum 6, pangkat d maksimum 10, dan pangkat p maksimum 14.
Angka n terbesar menunjukkan periode, untuk Lantanida periode 6, Aktinida periode 7.
Untuk Golongan A dan B, jumlah pangkat dari n terbesar menunjukkan nomor golongan.
Contoh Soal
Unsur pada atom 13Al dalam sistem periodik terletak pada …
Pembahasan :
Konfigurasi elektron yang terjadi adalah 13Al = 1s2 2s2 2p6 3s2 3p1 .
Dengan pola s dan p di paling kanan maka termasuk Golongan A.
Periode unsur adalah angka n terbesar yaitu 3.
Nomor golongan unsur adalah jumlah pangkat dari n terbesar yaitu 2+1 = 3 atau III.
Dengan demikian termasuk Golongan IIIA.